Pieprzyca, E., Skowronek, R., Nižnanský, Ľ., & Czekaj, P. (2020). Synthetic cathinones–From natural plant stimulant to new drug of abuse. European Journal of Pharmacology, 875, 173012.
Abstract.
Les cathinones de synthèse ont commencé à être utilisées comme substances récréatives au début du 21e siècle. Il existe encore peu de données sur ces composés, introduits sur le marché des drogues illicites pour la plupart après 2009. Étant donné que les cathinones de synthèse constituent actuellement le deuxième groupe le plus important de nouvelles substances psychoactives et dangereuses parmi plus de 670 nouvelles substances psychoactives identifiées en Europe et surveillées par l’OEDT, la recherche sur ces substances devrait être considérée comme extrêmement importante.
Cette revue se concentre sur la disponibilité des cathinones synthétiques sur le marché des drogues illicites, la présentation des tendances actuelles dans l’utilisation de ces substances, et leurs mécanismes d’action et de toxicité. Les auteurs discutent des cas d’intoxication aux cathinones synthétiques et des diagnostics post-mortem, ainsi que du problème de l’utilisation combinée de cathinones synthétiques avec d’autres substances psychoactives.
La littérature ainsi que les données cliniques et médico-légales indiquent la nécessité de poursuivre les recherches sur le métabolisme, la toxicocinétique, la toxicodynamique, les effets cliniques et le potentiel de dépendance des cathinones de synthèse, en particulier dans le contexte des menaces potentielles causées par l’augmentation de la consommation de ce groupe de drogues à l’avenir.
1. Introduction.
De nombreuses nouvelles substances psychoactives (NPS) ont été créées dans les années 1960 et durant le reste du 20e siècle. Bien qu’elles n’aient pas été spécifiquement appelées NPS, des analogues de drogues ont été continuellement développés pendant des décennies. En tant que substances récréatives, les NPS ont commencé à être utilisées à grande échelle au début du 21e siècle. L’Office des Nations unies contre la drogue et le crime (ONUDC) définit les NPS comme des “substances d’abus, soit sous forme pure, soit sous forme de préparation, qui ne sont pas contrôlées par la Convention unique sur les stupéfiants de 1961 ou la Convention sur les substances psychotropes de 1971, mais qui peuvent constituer une menace pour la santé publique”. Cette définition exclut donc toutes les substances classées au niveau international, y compris la 3,4-méthylènedioxyméthamphétamine (MDMA) et les amphétamines. Le terme “nouveau” ne fait pas nécessairement référence à de nouvelles inventions – plusieurs NPS ont été synthétisées pour la première fois il y a 40 ans – mais à des substances qui sont récemment devenues disponibles sur le marché (ONUDC). Ces composés agissent sur le système nerveux central (CNS) humain d’une manière similaire aux drogues connues depuis longtemps, comme l’amphétamine, le cannabis, l’héroïne ou le LSD. Les NPS constituent un groupe hétérogène de composés naturels, semi-synthétiques et synthétiques. Les NPS les plus populaires comprennent les cathinones synthétiques et les cannabinoïdes synthétiques. Au cours des dernières années, le marché des drogues illicites a connu une augmentation du nombre de psychostimulants connus sous le nom de substances psychoactives NPS, de drogues de synthèse, de sels de bain, d’aliments pour plantes, de produits chimiques de recherche, d’assainisseurs d’aspirateurs, de nettoyeurs d’étangs, de nettoyeurs de bijoux ou d’insectifuges.
Afin d’éviter toute responsabilité pénale, les préparations contenant des cathinones synthétiques portent généralement la mention “substance non adaptée à la consommation humaine”, “non testé pour la sécurité ou la toxicité”, “tenir hors de portée des enfants”, etc. Ces préparations sont achetées principalement sur des sites de vente en ligne et plus rarement dans des magasins ou directement auprès de personnes qui les distribuent. La composition des produits proposés sous les mêmes noms commerciaux peut varier en ce qui concerne la quantité (concentration) de substances psychoactives affectant le CNS et ils peuvent même contenir d’autres types de substances que celles spécifiées sur leurs étiquettes, ce qui signifie que leurs utilisateurs ne savent pas toujours quelle substance ils consomment et en quelle quantité. La qualité et la quantité des cathinones synthétiques disponibles sur le marché des drogues sont insuffisantes). De plus en plus, de nombreux produits contiennent non seulement des principes actifs uniques, mais aussi des combinaisons de deux dérivés ou plus. Ils comprennent souvent des mélanges, par exemple de caféine et de lidocaïne. Les cathinones synthétiques sont parfois vendues comme de la cocaïne ou de l’ecstasy (MDMA).
Sur le marché illicite, les cathinones de synthèse sont généralement distribuées sous forme de poudre blanche, de cristaux ou de gélules, la forme de comprimés étant moins populaire. Les cathinones synthétiques sont généralement prises par voie orale (gélules, solutions aqueuses et comprimés) et par voie nasale (sniffer une substance en poudre et l’absorber par la muqueuse nasale). Pour absorber une seule dose importante de cathinone synthétique, les usagers avalent la substance enveloppée dans du papier à cigarette (ce qu’on appelle le “bombing”). En raison de leur grande solubilité dans l’eau, les cathinones synthétiques sont également administrées par injection intraveineuse ou intramusculaire et utilisées sous forme de lavements. Il a été signalé que, dans certains cas, les injections intraveineuses étaient suivies de thromboses et d’embolies veineuses, ainsi que d’infections locales, d’abcès, de croûtes et de cicatrices. Les injecteurs d’opioïdes déclarent aussi souvent s’injecter des cathinones synthétiques. Plusieurs rapports ont mis en garde contre la popularité croissante de la consommation de cathinones de synthèse par voie intraveineuse. Les cathinones de synthèse sont parfois utilisées dans ce que l’on appelle les “sessions de méphédrone”, qui consistent à prendre des substances en plusieurs doses répétées en l’espace de quelques heures et généralement dans une situation sociale spécifique (par exemple, chez des amis, lors d’une fête à domicile ou dans des boîtes de nuit).
Les consommateurs de cathinones synthétiques invoquent un certain nombre de raisons pour expliquer la prise de ces substances, notamment le statut juridique (légalité), la disponibilité (achetées principalement sur Internet), le prix acceptable (inférieur à celui des drogues conventionnelles), l’absence de tests de dépistage rapides pour confirmer leur consommation, ou les préférences des consommateurs pour des propriétés pharmacologiques spécifiques, par exemple pour améliorer les expériences sociales et sexuelles.
En raison de leur statut légal initial, les cathinones de synthèse étaient considérées comme des “drogues légales” et souvent considérées par les usagers comme des alternatives sûres à d’autres stimulants couramment consommés. Les premières drogues de ce groupe sur le marché illicite ont été la méthcathinone et la 4-méthylméthcathinone (4-MMC, méphédrone), suivies par la 3,4-méthylènedioxyméthcathinone (MDMC, méthylone), la 3,4-méthylènedioxypyrovalérone (MDPV), la 4-méthoxyméthcathinone (méthédrone) et l’α-pyrrolidinopropiophénone (PPP). Au départ, la méphédrone et le MDPV étaient des cathinones que l’on trouvait le plus souvent dans les “sels de bain” en Europe. La méphédrone a gagné en popularité en raison, entre autres, de sa faible qualité et de la difficulté à obtenir de la cocaïne ou de la MDMA. La rapidité avec laquelle les cathinones de synthèse sont apparues dans la population des consommateurs de drogues et l’ampleur de leurs effets néfastes sur la santé ont conduit à l’introduction d’un contrôle légal de ces composés.
Actuellement, les cathinones de synthèse constituent le deuxième groupe le plus important de nouvelles substances psychoactives parmi plus de 670 NPS identifiées en Europe et surveillées par l’Observatoire européen des drogues et des toxicomanies (OEDT). Selon un rapport de l’OEDT, 130 cathinones de synthèse au total étaient enregistrées en Europe à la fin de l’année 2017 et 12 substances de ce type ont été identifiées pour la première fois cette année-là. En 2016, les cathinones de synthèse représentaient près d’un tiers (plus de 23 000) du nombre total de saisies de NPS. Le nombre total de cathinones de synthèse saisies avoisine 1,9 tonne, ce qui les place en première position sur la liste des NPS saisis en 2016.
Les rapports évaluant les données démographiques sur les consommateurs de cathinones synthétiques concluent que les personnes interrogées sont principalement de jeunes hommes. Un examen des données recueillies dans six pays de l’UE (Allemagne, Hongrie, Irlande, Pays-Bas, Pologne et Portugal) a révélé que la communauté Internet intéressée par le sujet des cathinones de synthèse était composée de personnes âgées de 18 à 25 ans ; toutefois, le profil des utilisateurs de cathinones de synthèse se situait plus probablement dans la tranche d’âge des 18-35 ans.
2. Propriétés chimiques.
Les cathinones synthétiques sont des analogues structurels de la cathinone, un alcaloïde psychostimulant présent dans le khat (Catha edulis). Le khat est connu et utilisé depuis des siècles par les populations d’Afrique de l’Est et du nord-est de la péninsule arabique en raison de ses propriétés psychoactives. Il a été découvert au Yémen au XVIIIe siècle par le botaniste Peter Forskal. Selon des références historiques, la pratique de la mastication des feuilles de khat pour leurs effets euphorisants et stimulants remonte à plusieurs siècles ; aujourd’hui, elle est toujours populaire dans des pays tels que la Somalie, le Yémen, le Kenya et l’Éthiopie. Les feuilles de khat contiennent de multiples composés, en particulier des alcaloïdes phénylalkylamines, dont la norpseudoéphédrine, la cathinone et la cathine. Ce n’est que dans les années 1970 que la cathinone, plus précisément le stéréo-isomère S-(-)-cathinone, a été isolée des feuilles de khat et considérée comme son principal composant psychoactif. La cathinone se décompose rapidement après la récolte des feuilles, c’est pourquoi les feuilles fraîches ne sont mâchées que dans les pays où la plante pousse ou dans les pays voisins. La muqueuse buccale joue un rôle important dans l’absorption des alcaloïdes. Les feuilles de khat sont également cuites occasionnellement dans la péninsule arabique et dans certaines régions d’Afrique de l’Est sous forme de thé. De nombreuses années avant la découverte de la cathinone dans le khat, le composé a été synthétisé par des chimistes médicaux.
2.1 Propriétés physico-chimiques des cathinones synthétiques.
Les cathinones synthétiques ont été synthétisées pour la première fois dans les années 1920 en tant que produits médicinaux potentiels. La première cathinone synthétique – la méthcathinone – a été produite en 1928, suivie par la méphédrone un an plus tard.
Toutes les cathinones synthétiques se caractérisent par la présence d’un groupe cétone en position β de la chaîne latérale (Fig. 1A). Les substituants (R1-R5) sont le plus souvent des atomes d’hydrogène ou des chaînes aliphatiques simples, mais aussi, entre autres, des anneaux de pyrrolidine ou des groupes halogènes.
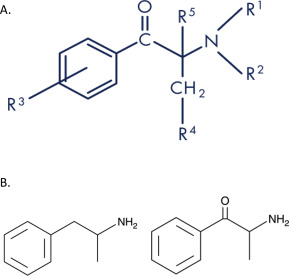
La structure chimique des cathinones synthétiques est similaire à celle de l’amphétamine, de la méthamphétamine et de l’ecstasy, raison pour laquelle elles sont communément appelées β-cétoamphétamines (Fig. 1B). Toutes les cathinones synthétiques sont basées sur la structure de base de la cathinone naturelle et sont des dérivés des phénylalkylamines, dont la structure ressemble à celle de la molécule d’amphétamine avec une liaison carbonyle en position β de la chaîne amino-alkylique substituée au niveau de l’anneau aromatique.
D’un point de vue chimique, les dérivés de la cathinone peuvent être divisés en trois groupes. Le groupe 1 se compose de composés N-alkyle ou de composés comportant un substitut alkyle ou halogène à n’importe quelle position de l’anneau aromatique. Il comprend les premières cathinones synthétiques, c’est-à-dire la buphedrone, l’ethcathinone, l’ephedrone, la flephedrone, la mephedrone et la pentedrone. Le groupe 2 comprend des composés méthylènedioxy-substitués à n’importe quelle position du cycle aromatique, tels que la butylone, la méthylone et la pentylone. Du point de vue de leur structure, ces composés ressemblent davantage à la MDMA et présentent une activité similaire. Les dérivés de la cathinone du groupe 3 sont des analogues des dérivés de la pyrrolidine tels que la 3,4-méthylènedioxyalphapyrrolidinopropiophénone (MDPPP) et la MDPV susmentionnée.
2.2 Méthodes analytiques d’identification.
Les NPS sont de plus en plus populaires et les tests de détection de leur présence dans le matériel biologique devraient faire partie des analyses de routine commandées par les autorités chargées de l’application de la loi. Il convient également de tenir compte du fait que certaines cathinones sont instables dans les matrices biologiques. Le matériel biologique collecté peut être influencé par diverses conditions pendant le transport, le stockage et l’analyse des échantillons, ce qui peut entraîner des changements significatifs dans la concentration des xénobiotiques avant leur analyse. L’analyse de la stabilité des cathinones synthétiques dans le sang à des températures de -20 °C, 4 °C, 20 °C et 32 °C a montré qu’elle dépendait non seulement de la température de stockage du matériel biologique, mais aussi de la structure chimique d’une substance donnée, et notamment de la présence de substituants dans le cycle aromatique et au niveau de l’atome d’azote. À une température de 32 °C, une perte significative d’analyte a été observée en quelques heures seulement. Des études similaires menées sur des échantillons d’urine ont montré que la stabilité des cathinones synthétiques dépendait du pH de l’urine et de la température de stockage. Les cathinones étaient beaucoup plus stables dans l’urine acide (pH = 4) et dans des conditions de basse température. Dans l’urine alcaline (pH = 8) et à une température de 32 °C, une perte importante d’analyte (>20 %) a été observée en quelques heures seulement.
Actuellement, parmi les méthodes de recherche utilisées pour analyser les drogues de synthèse, y compris les cathinones synthétiques, seules les techniques chromatographiques avancées permettent d’identifier et de quantifier sans ambiguïté les substances psychoactives dans le matériel biologique prélevé sur des personnes vivantes ou récupéré lors d’une autopsie. Les laboratoires de toxicologie médico-légale utilisent le plus souvent la chromatographie liquide et gazeuse couplée à la spectrométrie de masse (LC-MS et GC-MS).
Les problèmes analytiques liés à l’identification des substances psychoactives qui font partie des “drogues de synthèse” résultent principalement du nombre important et en constante augmentation de ces substances sur les marchés mondiaux et nationaux des drogues. Outre leur diversité, les NPS posent également de grandes difficultés analytiques en raison de leur action sur l’organisme à faibles doses et des changements métaboliques rapides et nombreux qu’elles subissent dans l’organisme. Il en résulte de faibles concentrations de composés d’origine et de leurs nombreux métabolites dans le matériel biologique. Par conséquent, la méthodologie utilisée dans les laboratoires de toxicologie doit être régulièrement mise à jour pour suivre l’évolution rapide du marché.
L’une des principales difficultés de l’analyse toxicologique est de distinguer les composés ayant des structures chimiques similaires, y compris les isomères structuraux, c’est-à-dire les composés chimiques ayant des formules moléculaires identiques, mais qui diffèrent par le type, l’ordre ou la disposition spatiale des liaisons atomiques. Cette difficulté est illustrée par l’exemple de la 4-chlorométhcathinone (clephedrone, 4-CMC) et de ses isomères, la 2-CMC et la 3-CMC, présentés dans la figure 2.
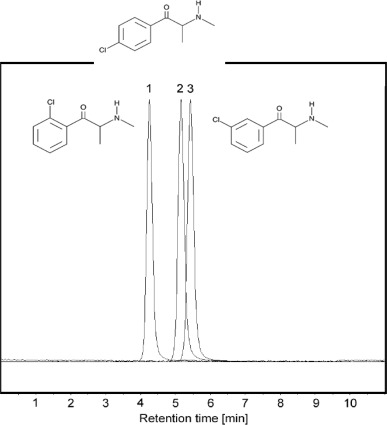
Ces composés ne diffèrent que par l’emplacement du groupe méthyle dans l’anneau benzénique de leur structure, ce qui génère des propriétés chimiques similaires, mais aussi des propriétés analytiques (chromatographiques) similaires sur la base desquelles nous identifions définitivement une substance donnée. Malgré leurs similitudes structurelles, les isomères de position peuvent présenter des propriétés pharmacologiques différentes et une toxicité sensiblement différente. La séparation et l’identification correcte des isomères sont également extrêmement importantes en ce qui concerne le statut juridique d’une substance donnée, qui peut varier.
3. Effets pharmacocliniques.
Chaque année, jusqu’à plusieurs dizaines de substances psychoactives arrivent sur le marché des médicaments pour lesquelles il existe peu ou pas de données bibliographiques concernant leur physicochimie, leur pharmacologie ou leur toxicité. On manque de données détaillées sur les effets des cathinones synthétiques sur le corps humain, bien que l’on sache qu’elles présentent de nombreux effets structurels, pharmacologiques et comportementaux similaires à ceux de l’amphétamine et de ses dérivés.
Certaines cathinones, par exemple les dérivés de la pyrovalérone, ont été synthétisées à l’origine comme nouveaux agents thérapeutiques, mais elles ont ensuite été retirées du marché et classées comme NPS. Comme l’amphétamine, la cathinone et ses dérivés synthétiques augmentent les niveaux de monoamines cérébrales, telles que la noradrénaline (NE), la sérotonine (5-HT) et la dopamine (DA). À l’instar des phénéthylamines, telles que la MDMA, les cathinones synthétiques peuvent avoir des propriétés similaires à celles des amphétamines et la capacité de moduler la 5-HT, ce qui se traduit par des effets psychoactifs prononcés. La plupart des dérivés de la cathinone ont des effets sympathomimétiques. D’autres qualités, notamment la durée et l’étendue des effets psychoactifs, varient largement en fonction de la structure du groupe fonctionnel. Par exemple, le raccourcissement de la chaîne alkyle réduit l’activité du transporteur de dopamine. Il a également été démontré que les cathinones synthétiques sont plus hydrophiles que leurs homologues amphétaminiques et sont moins capables de traverser la barrière hémato-encéphalique.
L’utilité des cathinones de synthèse en médecine a été étudiée principalement en termes d’utilisation de ces composés comme antidépresseurs et médicaments anorexigènes. Le diéthylpropion, également connu sous le nom d’amfépramone, qui est un analogue N,N-diéthyle de la cathinone, a été développé comme agent anorexigène au début des années 1960 par la société pharmaceutique allemande Temmler-Werke et est toujours prescrit dans certains pays sous le nom de Tenuate, une préparation efficace pour la perte de poids. La pyrovalérone a été étudiée comme agent antifatigue dans les années 1960. Le bupropion est un analogue N-tert-butyl de la cathinone qui a d’abord été étudié comme antidépresseur dans les années 1970 par Burroughs Wellcome (aujourd’hui GlaxoSmithKline), puis approuvé pour un usage clinique sous le nom de Wellbutrin. Le bupropion a également été approuvé en tant qu’aide au sevrage tabagique sous le nom de Zyban en 1997. En 2016, le bupropion était le cinquième médicament psychiatrique le plus prescrit aux États-Unis.
Les consommateurs de NPS psychoactifs en attendent un certain nombre d’effets, en particulier la bonne humeur, une plus grande confiance en soi, l’euphorie, la facilité de communication interpersonnelle, une perception sensuelle accrue et une plus grande ouverture d’esprit dans l’expression de ses sentiments, une énergie et une activité psychophysique accrues, une concentration accrue, une “clarté de pensée”, une amélioration des fonctions cognitives et de la capacité de mémorisation, ainsi qu’une réduction de la somnolence.
Récemment, une nouvelle tendance est apparue, consistant à s’injecter des drogues illégales, y compris des cathinones de synthèse, dans un contexte spécifique, une pratique que l’on appelle le “slamming”. Ce terme désigne l’injection intraveineuse de substances psychoactives lors d’événements où les gens ont des rapports sexuels afin d’augmenter le désir et le plaisir sexuels. En général, cela se passe lors des soirées dites “chem-sex”, où les cathinones de synthèse sont utilisées simultanément ou en combinaison avec d’autres substances psychoactives, telles que la méthamphétamine, le GHB/GBL, la cocaïne ou le sildénafil (Viagra). Ces événements peuvent durer de plusieurs heures à trois jours, et les participants adoptent souvent des comportements sexuels à risque, comme la non-utilisation de préservatifs et les rapports sexuels avec de nombreux partenaires occasionnels. Ces comportements à risque peuvent entraîner des problèmes médicaux et psychiatriques courants associés à la consommation de drogues par voie intraveineuse, notamment la contraction de maladies sexuellement transmissibles (MST) ou d’infections virales, telles que le virus de l’immunodéficience humaine (VIH) et le virus de l’hépatite C (VHC). Ces complications ne sont pas liées aux effets pharmacologiques des cathinones, mais aux voies d’administration et au manque de stérilité.
Les effets récréatifs susmentionnés des cathinones synthétiques ont été observés chez les utilisateurs, en particulier dans les groupes d’âge plus jeunes. Cependant, les cathinones synthétiques exercent une variété d’effets néfastes, voire toxiques, sur le corps humain. Parmi eux, les plus fréquemment signalés sont les symptômes cardiovasculaires, tels que la tachycardie, l’augmentation de la pression artérielle, les palpitations, les douleurs thoraciques, la myocardite et l’arrêt cardiaque ; les symptômes neurologiques, tels que l’insomnie, les maux de tête, le grincement des dents, les convulsions, les troubles visuels et la paresthésie ; et d’autres, tels que les saignements de nez, les ulcérations des muqueuses du nez et de la gorge, la dégradation des muscles squelettiques (rhabdomyolyse), et les lésions rénales. D’autres effets possibles sont la coagulation intravasculaire disséminée (CIVD) et la défaillance de plusieurs organes pouvant entraîner la mort. Dans le cas de la méphédrone et du MDPV, des complications thromboemboliques et des infections locales (y compris la fasciite nécrosante) ont été signalées.
Les changements de comportement et de perception du monde qui surviennent après la prise de cathinones synthétiques et qui vont au-delà de ceux attendus par le consommateur comprennent une variété de troubles mentaux et cognitifs. Une personne sous l’influence de cathinones peut présenter de l’irritabilité, de l’agressivité (se manifestant parfois par une violence extrême), de l’automutilation, de l’anxiété, des attaques de panique, un manque de motivation, de l’anhédonie, de la dépression, des pensées et tentatives suicidaires, des délires paranoïaques, des hallucinations auditives et visuelles (souvent sous la forme de personnes qui représentent une menace, qui suivent l’utilisateur ou qui ont l’intention de le tuer) et même une catatonie. En ce qui concerne le CNS des personnes intoxiquées, les symptômes identifiés jusqu’à présent comprennent, entre autres, la confusion, l’agitation, la psychose, les crampes musculaires, les vertiges, les acouphènes, les troubles de la mémoire à court terme, le parkinsonisme, les automatismes moteurs, l’œdème cérébral, les comportements violents et la dépendance.
En tant que substances psychoactives et récréatives, les cathinones présentent un potentiel d’abus important, ce qui a été confirmé par des études comportementales chez l’animal et chez l’homme. Une étude réalisée par Aarde et al. a mis en évidence un risque d’abus de type stimulant pour la 4-MMC dans le modèle préclinique traditionnel d’auto-administration chez le rat. Dans une autre étude, des rats Wistar femelles se sont auto-administrés par voie intraveineuse les stimulants substitués à la cathinone que sont la méphédrone et la méthylone, ainsi que la MDMA. Sur la base des résultats obtenus, il a été prédit que la responsabilité de ces trois composés est similaire chez les consommateurs de stimulants établis, mais qu’elle peut différer s’il s’agit de drogues primaires d’initiation. En outre, des rapports de cas ont été publiés sur des patients répondant aux critères actuels du DSM-5 pour les troubles liés à l’utilisation de substances. Les cathinones peuvent induire un état de manque important similaire à celui des drogues classiques et d’autres symptômes de sevrage, tels que des troubles du sommeil, de l’anxiété, de la dépression, de la méfiance, des tremblements, voire un comportement de type psychotique (délires et/ou hallucinations).
Les cathinones synthétiques peuvent également induire des symptômes psychotiques similaires aux symptômes positifs de la schizophrénie. Selon John et al, l’abus de cathinones synthétiques (sels de bain) doit faire partie du diagnostic différentiel lorsque la psychose est d’apparition récente ou cliniquement incongrue par rapport à la présentation primaire connue d’un trouble psychotique. Les personnes sous l’influence de cathinones synthétiques peuvent également avoir des pensées et des tendances suicidaires.
Les ensembles de symptômes cliniques indiquant une intoxication aux cathinones de synthèse (appelés toxidromes) se composent principalement de toxidromes sympathomimétiques et de toxidromes sérotoninergiques (tableau 1). Le toxidrome sympathomimétique est un ensemble hétérogène de symptômes cliniques résultant d’une très forte stimulation du système nerveux sympathique à la suite de la prise d’un xénobiotique sympathomimétique. Le syndrome sérotoninergique, quant à lui, comprend divers symptômes cliniques non spécifiques résultant de la stimulation de la transmission sérotoninergique dans le CNS et dans les tissus périphériques. Les symptômes associés aux toxidromes sympathomimétiques et sérotoninergiques sont similaires. Le diagnostic du syndrome sérotoninergique selon les critères de toxicité sérotoninergique de Hunter implique l’administration d’un agent sérotoninergique (par ex. cathinone synthétique) et l’apparition d’un ou plusieurs des symptômes suivants : (i) clonus spontané, (ii) clonus inductible ou oculaire avec agitation et diaphorèse, (iii) tremblements et hyperréflexie, ou (iv) hypertonie, hyperpyrexie (température de 38 °C) et clonus inductible ou oculaire.
| Type de toxidrome | Sympathomimétique | Sérotonine |
| Système nerveux | Agitation psychomotrice Tremblements, convulsions, hyperréflexie | État confusionnel, de la somnolence au coma, tension musculaire accrue |
| Pupilles | Dilatées | |
| Système cardiovasculaire | Tachycardie, augmentation de la pression artérielle | |
| Système respiratoire | Tachypnée | |
| Température | Elevée | |
| Autres | Anorexie, diaphorèse | Diaphorèse, diarrhée, blocage de mâchoire |
Lors des sessions de drogue, les cathinones synthétiques sont souvent prises avec des médicaments populaires et d’autres drogues, ce qui modifie de manière multidirectionnelle leur action aux niveaux somatique et mental, notamment avec de l’alcool et des bêta-bloquants (pour prévenir la tachycardie), du cannabis ou des dérivés de benzodiazépines (pour combattre l’anxiété), de la famotidine, de l’oméprazole ou de la dompéridone (pour inhiber la sécrétion d’acide gastrique et prévenir les douleurs abdominales), d’autres composés psychostimulants, p. ex. par exemple la cocaïne, l’amphétamine, le modafinil, la trifluorométhylphénylpipérazine ou la benzylpipérazine (pour augmenter la stimulation du CNS et l’empathie), et la kétamine ou la zopiclone (pour intensifier les hallucinations visuelles).
Des études expérimentales in vivo sur des animaux confirment que les cathinones synthétiques, probablement en agissant sur les systèmes monoaminergiques centraux, provoquent de profonds changements comportementaux chez les animaux. Den Hollander et al. ont étudié les effets possibles à long terme de la méphédrone et de la méthylone sur la mémoire, l’anxiété et la dépression chez la souris, ainsi que les effets à long terme de ces substances sur la neurochimie du cerveau chez le rat et la souris. La méphédrone et la méthylone ont été administrées deux fois par jour pendant 4 jours à des doses de 30 mg/kg. Après deux semaines, des tests comportementaux ont été effectués pour évaluer les effets de ces substances sur la mémoire, l’anxiété et la dépression ; en outre, les niveaux de DA, de 5-HT et de leurs métabolites, ainsi que de NE, ont été mesurés dans le cerveau des animaux. Il a été démontré que la méphédrone réduisait les performances de la mémoire de travail mais n’affectait pas les niveaux de neurotransmetteurs, à l’exception d’une baisse de 22 % de la concentration d’acide homovanillique (HVA) chez les souris. La méthylone a eu peu d’effet sur le comportement et les niveaux de neurotransmetteurs chez les souris, mais a provoqué une déplétion généralisée des niveaux de 5-HT et de 5-HTTT chez les rats. La méthylone et la méphédrone se sont toutes deux révélées avoir des effets à long terme sur les indicateurs comportementaux et biochimiques de la neurotoxicité chez les rongeurs.
Il a également été démontré que la méphédrone, la méthylone et le MDPV augmentent rapidement l’activité locomotrice d’une manière décrite comme des épisodes récurrents d’hyperlocomotion séparés par de brèves périodes de repos. Des différences dans les activités locomotrices de la méphédrone et du MDPV ont été observées en fonction de la dose appliquée d’une cathinone synthétique. La méphédrone diminue de manière dose-dépendante l’intensité et la durée de la course volontaire sur roue, alors que de faibles doses de MDPV augmentent l’intensité et la durée de cette activité.
Malgré la perte des capacités motrices, les animaux recevant de la méphédrone ont montré une légère amélioration de la croissance de la mémoire visuospatiale. Cependant, l’amélioration à court terme de la mémoire visuospatiale peut ne pas persister sur de longues périodes ou lors d’une exposition chronique à la méphédrone. L’administration de méphédrone pendant plusieurs jours a entraîné une altération de la mémoire de travail chez les souris. Les rats juvéniles recevant de la méphédrone sur des périodes prolongées ont également montré une détérioration de la mémoire de travail à long terme. Bon nombre de ces observations ont été faites chez des personnes consommant de la méphédrone, mais les effets à long terme de la consommation de méphédrone sur la mémoire et le comportement humains sont inconnus.
Par ailleurs, de récentes études animales utilisant le MDPV ont confirmé que la prise de cette substance peut entraîner des déficits dans la reconnaissance des objets et la mémoire de travail. L’étude de Sewalia et al. a utilisé un modèle de rat Sprague-Dawley d’auto-administration volontaire à long terme de MDPV de type binge en cinq sessions de 96 heures. Comparativement aux animaux s’auto-administrant une solution saline, les animaux s’auto-administrant du MDPV ont montré (1) une prise de drogue robuste qui s’est intensifiée au fil du temps, (2) des déficits dans la reconnaissance d’objets nouveaux, mais pas dans la reconnaissance d’objets spatiaux, et (3) une neurodégénérescence dans les cortex périrhinaux et entorhinaux. Bernstain et al. ont prouvé que l’exposition chronique des animaux au MDPV produit une dysrégulation spécifique au site des marqueurs de la dopamine dans le circuit mésocorticolimbique et des déficits de mémoire dans le test de reconnaissance d’objets nouveaux qui sont influencés par les récepteurs D1.
4. Toxicité.
La toxicité des cathinones synthétiques est directement liée à la structure (composition chimique) d’une substance donnée et dépend également de la dose absorbée d’une substance unique ou d’un mélange. Les mécanismes d’action des cathinones synthétiques sont étudiés dans des modèles animaux expérimentaux et dans des cultures cellulaires in vitro. Cependant, seul un nombre limité de ces composés a été testé (tableau 2). L’analyse des résultats de ces études est complexe, non seulement en raison des différences entre les expériences menées, mais aussi en raison de l’utilisation, dans des études individuelles, de diverses substances du groupe des cathinones synthétiques, généralement celles qui sont les plus populaires sur le marché des drogues illicites. Un certain nombre de descriptions dans la littérature des effets toxiques causés par les cathinones synthétiques se rapportent à ce que l’on appelle la première génération, qui comprend la 4-MMC, la MDMC et la MDPV. À ce jour, aucun test in vitro n’a été réalisé sur certaines cathinones de synthèse, même sur des substances identifiées sur le marché des drogues illicites avant 2010, notamment l’éthcathinone, la diméthylcathinone (métamfépramone) et la benzédrone. Il n’y a pas beaucoup de données même pour la nouvelle génération de cathinones synthétiques, comme la N-propylcathinone, la 4-fluoroethcathinone et la 3′,4′-triméthylène-α-éthylaminovalérophénone.
[TABLEAU 2]
4.1 Mécanisme d’action des cathinones de synthèse, en particulier sur le CNS.
Les mécanismes moléculaires d’action des cathinones de synthèse imitent l’action des drogues classiques et reposent principalement sur l’augmentation de la concentration extracellulaire des neurotransmetteurs monoaminergiques : DA, NE et 5-HT.
Généralement, compte tenu du mécanisme d’action et de la similitude avec les drogues classiques, les cathinones synthétiques sont divisées en trois sous-groupes.
- Le premier sous-groupe est constitué de cathinones ayant des effets similaires à ceux de la cocaïne et de l’ecstasy (par exemple, la méphédrone, la méthylone, l’éthylone et la butylone). Comme la cocaïne, ces composés inhibent la recapture des monoamines, en particulier de la DA. En outre, ils imitent l’action de l’ecstasy en stimulant la libération de 5-HT.
- Le deuxième sous-groupe est constitué des cathinones de type méthamphétamine (par exemple méthylcathinone et flephedrone) qui, comme l’amphétamine et la méthamphétamine, inhibent la recapture de la DA et de la NA et stimulent la libération de la DA.
- Le troisième sous-groupe est constitué par les cathinones pyrovalérones (par exemple MDPV, a-PVP, PV8), qui inhibent fortement la recapture de la DA et de la NA, mais n’affectent pas la libération des monoamines.
La régulation des concentrations de neurotransmetteurs monoaminergiques s’effectue principalement au niveau des protéines de transport membranaires responsables du transport inverse des neurotransmetteurs de la fente synaptique vers le neurone (respectivement, le transporteur de la dopamine – DAT, le transporteur de la noradrénaline – NET, et le transporteur de la sérotonine – SERT). Les composés qui sont des inhibiteurs des protéines de transport inhibent temporairement la recapture des monoamines de la fente synaptique vers le neurone et augmentent ainsi leur concentration dans la fente synaptique. Des études in vitro ont montré que la méphédrone et la méthylone inhibent le DAT, le SERT et le NET à des concentrations micromolaires, et que l’α-PVP et le MDPV sont des inhibiteurs puissants du DAT et du NET dans la gamme des nanomolaires. Les effets sur d’autres récepteurs de neurotransmetteurs (acide α-amino-3-hydroxy-5-méthyl-4-isoxazolepropionique – AMPA, cannabinoïde – CB, acide γ-aminobutyrique – GABAA, N-méthyl-D-aspartate – NMDA, récepteur nicotinique de l’acétylcholine – nACh-R) n’ont pas été rapportés.
Les cathinones synthétiques produisent divers effets sur les marqueurs de la fonction terminale monoaminergique ; elles peuvent augmenter la formation d’espèces réactives de l’oxygène et de l’azote, induire une signalisation apoptotique et provoquer une neurodégénérescence et une cytotoxicité. Certains éléments indiquent que la méphédrone, le MDPV et la méthylone modifient les niveaux de SERT et de DAT et sont donc susceptibles d’endommager ces terminaux nerveux ; toutefois, des études supplémentaires sur la neuroinflammation et la neurotoxicité induites par les cathinones synthétiques sont manifestement nécessaires.
Les cathinones synthétiques présentent généralement une faible affinité pour le récepteur 1 associé aux amines traces (TAAR1), qui est la cible d’autres amphétamines. Les exceptions sont la 2,4-diméthylméthcathinone et la 2,3-diméthylméthcathinone, qui présentent une affinité submicromolaire pour les récepteurs TAAR1 chez la souris et le rat.
Les substances psychoactives présentant des effets psychostimulants et euphorisants intensifient la transmission dopaminergique et noradrénergique, tandis que les substances empathogènes, telles que la MDMA ou la 3,4-méthylènedioxy-N-éthylamphétamine (MDEA), intensifient la transmission sérotoninergique. Le paramètre qui permet de prédire la nature d’une substance psychoactive est le rapport entre son affinité pour le DAT et son affinité pour le SERT (appelé rapport DAT/SERT). Plus la valeur est faible, plus la part de la composante sérotoninergique est importante (tableau 3). Certaines cathinones agissent également comme substrats des protéines de transport et, lorsqu’elles sont transférées à l’intérieur des neurones, libèrent en plus des neurotransmetteurs dans la fente synaptique.
[TABLEAU 3]
Dans le dernier rapport européen sur les médicaments, de nouvelles cathinones synthétiques sont apparues, telles que la 4-CMC et la 4-chloroéthcathinone (4-CEC). La 4-CMC est un dérivé de la méthcathinone para-halogénée. Luethi et al. ont publié une étude présentant le profil pharmacologique et la toxicité hépatocellulaire des amphétamines et cathinones para-halogénées. L’inhibition de l’absorption des monoamines a été évaluée dans des cellules rénales embryonnaires humaines transfectées (HEK 293) qui exprimaient le DAT, le SERT et le NET humains. Il a été montré que la 4-CMC et la flephedrone (4-fluorométhcathinone 4-FMC) inhibaient la recapture de la norépinéphrine et de la dopamine à des concentrations micromolaires. L’ordre de toxicité suivant a été observé pour les para-substituants : chlorure > fluorure > hydrogène.
Des résultats similaires ont été observés avec d’autres cathinones halogénées et des cathinones pyrovalérones. La méthcathinone, la 4-fluorométhcathinone, la 4-bromométhcathinone, la 4-éthylméthcathinone, la 4-méthylméthcathinone, la pyrovalérone, la 3,4-méthylènedioxy-alpha-pyrrolidinopropiophénone (MDPPP), la 3,4-méthylènedioxy-alpha-pyrrolidinobutiophénone (MDPBP), le MDPV, la naphyrone et l’α-PVP ont été testés pour les monoamines libérées : 5-HT, DA et NE, ainsi que l’inhibition du transporteur de recapture des monoamines comme marqueurs de toxicité. La toxicité a été évaluée sur des cellules 293 (HEK 293). La 4-méthylméthcathinone, la 4-éthylméthcathinone, la 4-bromométhcathinone et la 4-fluorométhcathinone ont libéré de la 5-HT, de la DA et de la NE. La méthcathinone ne libère que de la DA et de la NE. Cela suggère que la para-halogénation ou la para-addition des groupes méthyle et éthyle à la méthcathinone agissent sur la libération de 5-HT. La pyrovalérone et les cathinones de type pyrovalérone (MDPPP, MDPBP, MDPV, naphyrone, α-PVP) n’ont pas libéré de DA, NE ou 5-HT. La 4-bromométhcathinone et la 4-éthylméthcathinone étaient des inhibiteurs très puissants de la NET, de la DAT et de la SERT. Les inhibiteurs très puissants de la NET aux concentrations les plus faibles étaient la méthcathinone, la 4-fluorométhcathinone, la 4-bromométhcathinone et la 4-méthylméthcathinone. La méthcathinone, la 4-méthylméthcathinone et la 4-fluorométhcathinone étaient des inhibiteurs plus puissants de la DAT que la 4-bromométhcathinone et la 4-éthylméthcathinone. La méthcathinone, la 4-méthylméthcathinone et la 4-fluorométhcathinone étaient de moins bons inhibiteurs de la 5-HT que la 4-bromométhcathinone et la 4-éthylméthcathinone. Toutes les cathinones à base de pyrovalérone étaient de très puissants inhibiteurs des transporteurs de catécholamines (NET et DAT) avec une très faible activité sérotoninergique. Il convient de considérer que si des cathinones synthétiques sont impliquées dans l’inhibition de la libération de monoamines, elles pourraient être de puissants inhibiteurs du transporteur de monoamines correspondant. Cependant, des études plus détaillées sont nécessaires pour prouver cette hypothèse.
Il convient également de noter qu’un certain nombre d’études ont montré que les métabolites actifs du MDPV et de la méphédrone sont d’importants modulateurs de l’action des transporteurs de catécholamines. Des tests effectués sur des échantillons biologiques ont montré que le MDPV est métabolisé en 3,4-dihydroxypyrovalérone (3,4-catéchol-PV) et en 4-hydroxy-3-méthoxypyrovalérone (4-OH-3-MeO-PV). Le principal métabolite du MDPV est le 4-OH-3-MeO-PV, qui s’est avéré être un faible bloqueur dans les essais d’inhibition de l’absorption pour le DAT et le NET. D’autre part, le 3,4-catéchol-PV est un puissant bloqueur de l’absorption au niveau du DAT in vitro, mais n’a qu’une faible activité après administration in vivo. Ces résultats montrent que le MDPV et ses métabolites actifs représentent une classe unique d’inhibiteurs de transporteurs à fort potentiel addictif.
D’autre part, la méphédrone agissant comme un libérateur de type substrat au niveau du DAT, du NET et du SERT est métabolisée en plusieurs composés de phase I, notamment la 4-méthylcathinone (nor-méphédrone), la 4-hydroxytolylméphédrone (4-OH-méphédrone) et la dihydroméphédrone. Il a été démontré que ces métabolites de la méphédrone sont des substrats du transporteur (c’est-à-dire des libérateurs) au niveau du DAT, du NET et du SERT, bien que la dihydroméphédrone soit faible à cet égard. Administrée in vivo, la nor-méphédrone augmente la dopamine et la 5-HT extracellulaires dans le cerveau, contrairement à la 4-OH-méphédrone. Cela suggère que la 4-OH-méphédrone ne pénètre pas la barrière hémato-encéphalique.
Wojcieszak et al. ont mené une étude sur la cytotoxicité des cathinones synthétiques du groupe des dérivés de l’α-pyrrolidinophénone, notamment l’α-PVP, le PV8 et le PV9, ainsi que leurs dérivés 4-fluoro- et 4-méthoxy. L’étude a été menée sur des modèles de lignées cellulaires du système nerveux (SH-SY5Y), du foie (Hep G2) et de l’épithélium des voies aériennes supérieures (RPMI 2650) ainsi que sur des cardiomyocytes (H9C2(2-1)). Les chercheurs ont examiné l’effet des pyrovalérones sur la fluidité de la membrane plasmique comme mécanisme potentiel de leur cytotoxicité. L’étude a démontré que les α-pyrrolidinophénones avec des chaînes latérales plus longues et leurs dérivés fluorés et méthoxylés produisent une cytotoxicité maximale plus importante en ce qui concerne l’activité mitochondriale et l’intégrité de la membrane cellulaire que l’α-PVP à cinq atomes de carbone et ses dérivés substitués. Il a également été prouvé que les changements de fluidité de la partie intérieure de la membrane plasmique contribuent à la cytotoxicité des dérivés de la pyrovalérone.
4.2 Effets toxiques sur le système cardiovasculaire.
On sait aujourd’hui qu’outre le CNS, les organes particulièrement vulnérables aux effets toxiques des cathinones de synthèse sont le cœur et les reins.
En ce qui concerne le système cardiovasculaire des personnes intoxiquées, les symptômes identifiés jusqu’à présent comprennent, entre autres, la tachycardie, l’hypertension, les douleurs thoraciques, l’arythmie cardiaque, l’infarctus du myocarde et la myocardite. Les effets toxiques des cathinones synthétiques sur le muscle cardiaque peuvent, dans des cas extrêmes, entraîner une mort cardiaque subite due à des changements fonctionnels ainsi qu’à des changements organiques, provenant par exemple d’une ischémie myocardique précoce ou d’une réponse inflammatoire focale. Les symptômes signalés par les personnes intoxiquées et observés par le personnel médical ne sont pas spécifiques : dyspnée, douleurs thoraciques, tachycardie et bradycardie, hyper- et hypotension, etc.
La cause sous-jacente des décès “électriques” dus à des arythmies mortelles est le fait que les cathinones synthétiques peuvent allonger l’intervalle QT sur l’ECG, favorisant la tachycardie ventriculaire polymorphe de type torsade de pointes, qui, à son tour, peut provoquer une syncope et une mort cardiaque subite, même chez des personnes jeunes et en bonne santé. Ces symptômes surviennent le plus souvent lors d’un effort physique ou d’un stress important. En outre, les ECG de personnes intoxiquées par des NPS ont montré, entre autres, une tachycardie, des modifications du segment ST, une fibrillation auriculaire et même une asystolie.
Pour ces raisons, lors de l’examen et de l’autopsie, mais aussi lors des examens complémentaires des personnes suspectées d’intoxication aux NPS, il convient d’accorder une attention particulière à la présence de pathologies dans le myocarde. Il est évident que des recherches supplémentaires sont également nécessaires sur le mécanisme de cardiotoxicité de ces agents, ainsi que la notification de chaque cas de décès cardiaque confirmé par analyse dans le cadre d’une intoxication aux cathinones synthétiques.
4.3 Effets toxiques sur les reins.
Les cathinones de synthèse peuvent également provoquer des nausées, des vomissements, des douleurs abdominales, des troubles de la motilité intestinale, une hyponatrémie, une hypokaliémie, une acidose, une rhabdomyolyse et des lésions rénales aiguës.
Les reins, en tant qu’organes impliqués dans le métabolisme et l’excrétion des xénobiotiques, sont particulièrement vulnérables aux effets toxiques primaires et secondaires des NPS. Les lésions rénales aiguës (IRA) sont le plus souvent secondaires à une rhabdomyolyse non traumatique, qui survient en raison de crises d’épilepsie, d’une activité musculaire excessive (également au cours d’une agitation psychomotrice), de l’effet toxique d’une substance sur les myocytes squelettiques ou d’une combinaison de plusieurs des causes susmentionnées. Elle s’accompagne généralement d’une déshydratation et d’une hyperpyrexie (température corporelle supérieure à 41,1 °C). L’IRA primaire sous forme ischémique après l’utilisation de cathinones synthétiques est généralement causée par une nécrose tubulaire aiguë due à l’action vasoconstrictrice des cathinones. L’effet néphrotoxique direct de ce groupe de substances synthétiques ne peut pas non plus être exclu.
Les cliniciens soulignent que les diagnostics différentiels des lésions rénales aiguës inexpliquées, en particulier chez les jeunes, doivent prendre en compte les effets indésirables des NPS, même en cas de résultats négatifs des tests toxicologiques. Du point de vue médico-légal, il est important de procéder à une analyse pré-mortem des résultats des tests de laboratoire de la fonction rénale si la personne intoxiquée a été hospitalisée et d’effectuer une évaluation histopathologique approfondie en distinguant les changements non mortels de ceux qui peuvent être un “artefact” posthume.
5. Intoxication aux cathinones.
5.1 Intoxications non mortelles et interprétation des concentrations.
L’aspect le plus important de la détection toxicologique médico-légale des cas d’intoxication aiguë est la détermination des taux de cathinone dans le sérum. Par exemple, Beck et al. ont présenté 114 cas d’intoxication par des cathinones synthétiques, confirmés analytiquement dans l’urine ou le sérum des patients. Outre le MDPV et l’α-PVP, qui étaient les plus populaires, onze autres dérivés de la pyrovalérone ont été trouvés. Les suivants ont été déterminés le plus souvent : 4′-fluoro-α-pyrrolidinopentiophénone (4F-alpha-PVP, fourchette 23-43 ng/ml), alpha-pyrrolidinohexiophénone (alpha-PHP, fourchette : 4-10 ng/ml), alpha-pyrrolidinobutiophénone (alpha-PBP, fourchette : 2-436 ng/ml), 3′,4′-méthylènedioxy-alpha-pyrrolidinohexiophénone (MDPHP, plage : 3-136 ng/ml), alpha-pyrrolidinopentiothiophénone (alpha-PVT, plage : 8-1 060 ng/ml) et 4′-fluoro-alpha-pyrrolidinohexanophénone (4F-alpha-PHP, plage : 3-28 ng/ml). Toutes ces substances ont également été dosées dans l’urine, mais le résultat du dosage dans cette matière biologique n’est pas un marqueur d’intoxication aiguë.
L’analyse des concentrations susmentionnées de cathinones dans le sérum permet d’affirmer que la gamme des cathinones synthétiques est très variée et qu’il est difficile de déterminer les concentrations toxiques et létales. Toutefois, il convient de rappeler que certains de ces cas auraient été fatals sans la mise en œuvre rapide de soins médicaux intensifs en milieu hospitalier. Certains cas concernaient des personnes chroniquement dépendantes, qui ont donc fait preuve de tolérance à la drogue. En outre, certains cas incluaient également d’autres substances psychoactives, ce qui complique l’interprétation. Chez 8 patients seulement, une seule substance a été détectée dans le sérum et l’urine : alpha-PBP (161 ng/ml dans le sérum, 305 ng/ml dans l’urine), MDPHP (<1-14,3 ng/ml dans le sérum, 19-305 ng/ml dans l’urine), 4F-alpha-PVP (43 ng/ml dans le sérum), alpha-PVT (425 ng/ml dans le sérum), et alpha-PHP (1,9 ng/ml dans le sérum, 3 ng/ml dans l’urine). Les concentrations déterminées dans les cas d’intoxications simples avec un seul dérivé de la pyrovalérone, qui n’ont pas entraîné la mort, étaient significativement plus faibles que celles rapportées dans les cas d’intoxications mixtes avec plusieurs substances. Dans ces cas, les observations cliniques ont montré une agitation psychomotrice, des douleurs musculaires, une hypothermie, une hypertension, des hallucinations, une mydriase, une tachycardie, un comportement agressif, des troubles de l’élocution et des paresthésies. Ces symptômes dépendaient du moment de la prise d’une substance donnée. Les observations ci-dessus concernant les symptômes d’intoxication sont cohérentes avec les conclusions d’autres études sur l’impact des NPS sur les différents systèmes de l’organisme humain.
Ces dernières années, les cathinones de synthèse, seules ou en mélange, ont été de plus en plus souvent détectées chez les conducteurs de différents pays. Étant donné que l’utilisation de cathinones synthétiques peut provoquer divers types de troubles mentaux, comme la paranoïa et les hallucinations, leur consommation par les conducteurs peut entraîner de graves accidents de la circulation et la mort des participants. Chez 28 conducteurs polonais, où l’α-PVP était la seule substance psychoactive détectée, la concentration sanguine était comprise entre 6,4 et 71 ng/ml. Aucun symptôme n’a été observé chez tous les conducteurs. Des symptômes tels qu’une démarche chancelante, la confusion, la volubilité, la surprise, la confusion, des troubles de l’élocution, un réflexe pupillaire lent, une rougeur de la peau du visage et des pupilles larges ou étroites sont apparus lorsque la concentration sanguine d’α-PVP se situait entre 8,2 et 68 ng/ml. Zawilska et al. ont examiné 24 cas de conduite sous l’influence de divers dérivés de la pyrovalérone. L’α-PVP a été détecté dans 8 cas et ses concentrations étaient comprises entre 32 et 230 ng/ml. Le MDPV seul n’était présent que dans un cas et sa concentration sanguine était de 60 ng/ml. D’autres dérivés de la pyrovalérone étaient présents en combinaison avec d’autres substances. Dans un cas, la méthylone a été détectée dans le sang à une concentration de 6,1 ng/ml et l’α-PVP à une concentration de 63 ng/ml. Dans d’autres études, le MDPV a été trouvé dans le sang à une concentration de 6 ng/ml. En combinaison avec d’autres substances, les concentrations de MDPV allaient de <10 à 368 ng/ml. Deux cas ont été décrits, concernant des motocyclistes impliqués dans des accidents de la route. Dans le premier cas, outre le THC et le THC-COOH, l’étude a révélé la présence de MDPV et de méthylone dans le sang à des concentrations respectives de 56 ng/ml et 729 ng/ml. Dans le second cas, seul le MDPV a été trouvé dans le sang à une concentration de 31 ng/ml. Toutes ces études s’accordent à dire que dans les cas de conduite de véhicules à moteur sous l’influence de nouvelles substances psychoactives du groupe des cathinones, les NPS les plus fréquemment détectées sont les dérivés de la pyrovalérone.
5.2 Intoxications mortelles et diagnostic post-mortem.
Le nombre exact d’intoxications mortelles par des NPS reste inconnu pour un certain nombre de raisons. Premièrement, dans tous les cas de décès dus à une cause inconnue, une autopsie n’est pas ordonnée avec collecte de matériel biologique approprié pour des études toxicologiques spécialisées. Deuxièmement, même si ce matériel est obtenu, le bureau du procureur n’ordonne pas toujours les tests appropriés. Troisièmement, tous les laboratoires toxicologiques qui reçoivent ce matériel biologique ne sont pas en mesure de déterminer les NPS actuellement sur le marché. Quatrièmement, si une personne intoxiquée a été hospitalisée, le matériel biologique prélevé lors de l’autopsie peut ne plus contenir la substance à l’origine de la détérioration soudaine de l’état de santé.
La recherche de la cause et du mécanisme du décès en cas de suspicion d’intoxication mortelle aux cathinones de synthèse ne diffère pas du diagnostic post-mortem classique en médecine légale. De la même manière qu’en médecine clinique, il comprend une anamnèse (recueil des antécédents), un examen physique et des tests supplémentaires. Pour des raisons évidentes, un médecin légiste obtient des informations uniquement auprès de son client, qui est généralement un procureur, des dossiers mis à disposition par le client et – ce qui est important si la personne a été hospitalisée – des dossiers médicaux protégés. Idéalement, le médecin devrait se familiariser avec la documentation médicale avant l’examen et l’autopsie, qui sont l’équivalent d’un examen physique clinique. Cela permet d’adapter l’étendue de l’autopsie au cas particulier et de recueillir le matériel optimal pour les examens complémentaires.
Dans la pratique, le matériel pour les tests histopathologiques et toxicologiques complémentaires est le plus souvent réservé (y compris le matériel alternatif au sang, à l’urine et aux fragments de rein et de foie prélevés en routine, par exemple des échantillons de tissu adipeux, de cerveau, de poumons et de cheveux). Il est également possible d’effectuer des tests biochimiques, microbiologiques et génétiques post mortem, si nécessaire (par exemple en cas de suspicion de septicémie).
Malheureusement, il n’existe pas d’image caractéristique en coupe chez les personnes intoxiquées par des drogues de synthèse. Le plus souvent, les observations se limitent aux représentants de la mort subite avec des caractéristiques de l’insuffisance circulatoire aiguë sous forme d’œdème cérébral et pulmonaire, de congestion des organes internes et de fluidité sanguine. L’étendue des lésions rencontrées dépend principalement de l’âge de la personne décédée et de l’hospitalisation ou non de la personne intoxiquée. En cas d’hospitalisation de longue durée dans une unité de soins intensifs, des complications infectieuses sont souvent observées (par exemple, pneumonie au cours de la thérapie respiratoire, caractéristiques d’une infection généralisée).
L’analyse microscopique des sections d’organes internes prélevées lors de l’examen et de l’autopsie des victimes d’intoxication par des drogues de synthèse ne joue qu’un rôle auxiliaire, car même au niveau microscopique, il n’existe pas d’image morphologique caractéristique permettant de diagnostiquer l’intoxication.
Dans les cas d’intoxications mortelles, on tente de déterminer si la cathinone synthétique a été consommée seule ou mélangée à d’autres substances. La méphédrone, la méthédrone et la butylone sont souvent consommées avec d’autres drogues. Par exemple, des examens post-mortem ont révélé la présence de méphédrone en combinaison avec de l’alcool éthylique, de la 3-trifluorométhylphénylpipérazine, de la MDMA, de l’héroïne et de la cocaïne. Dans deux cas, la présence de méthédrone et de butylone a été détectée avec d’autres xénobiotiques. Dans tous ces cas, le décès était accidentel et la détection de plusieurs substances psychoactives a rendu difficile la détermination du rôle des cathinones synthétiques comme cause du décès.
L’étude la plus complète sur les décès associés à la consommation de cathinones de synthèse a été publiée par Kraemer et al. qui ont essayé de trouver tous les cas avec détermination des concentrations post-mortem de ces substances. Ainsi, le MDPV était présent dans 30 cas, dont quatre où il était le seul xénobiotique, et la MDMC a été détectée dans 16 cas, dont six sans substances psychoactives d’accompagnement. Les causes de décès étaient variées, mais dans presque tous les cas, les cathinones synthétiques ont été déterminées en même temps que d’autres drogues conventionnelles, de nouvelles substances synthétiques ou des médicaments. Par conséquent, l’interprétation du rôle des cathinones de synthèse dans le pathomécanisme du décès est un processus complexe. Dans chaque cas, il faut avant tout examiner des données précises sur la redistribution post-mortem, la pharmacocinétique, la pharmacodynamique, les méthodes validées de dosage des cathinones de synthèse et les interactions avec d’autres xénobiotiques. Ces types de données sont malheureusement encore très rares.
6. Effets combinés des cathinones synthétiques et d’autres substances psychoactives.
L’un des principaux problèmes de la toxicologie médico-légale moderne est invariablement l’abus de plusieurs substances psychoactives en même temps. Les raisons exactes pour lesquelles les consommateurs combinent plusieurs types de substances psychoactives restent inconnues. Malheureusement, les gens consomment des cathinones synthétiques en même temps que des cannabinoïdes synthétiques ou du cannabis, et les études animales sur les effets de ces combinaisons font encore défaut.
Certaines études permettent de comparer les mécanismes d’action pharmacologiques des NPS et des amphétamines, y compris la méthamphétamine et la MDMA. Par exemple, il a été démontré que le MDPV associé à la méthamphétamine a un effet opposé. Cela signifie que le MDPV n’est pas toxique pour les terminaux DA. La méthylone n’a pas d’effet nocif sur les terminaisons nerveuses de la dopamine. Cependant, comme dans le cas de la méphédrone, les effets neurotoxiques accrus de la méthamphétamine sont mis en évidence par une réduction plus importante des niveaux de TH, de DA et de DAT. Cela est en corrélation avec le phénomène répandu de polyconsommation d’une cathinone synthétique avec d’autres cathinones synthétiques ou des drogues conventionnelles, où l’effet sur l’homme ou l’animal est renforcé ou altéré.
Lopez-Rodriguez et Viveros ont résumé les interactions des cathinones de synthèse avec l’éthanol, le cannabis, les cannabinoïdes de synthèse, la cocaïne et la nicotine, car la nicotine et l’éthanol sont souvent consommés par les jeunes lors de fêtes et sont donc susceptibles d’être associés à des NPS tels que les cathinones de synthèse, contribuant potentiellement à l’état toxique de l’organisme. L’éthanol et la nicotine ainsi que les cathinones de synthèse étaient relativement souvent présents dans les cas post-mortem. Les effets de la combinaison de l’éthanol et de la méphédrone sur la libération de 5-HT et de DA ont été testés dans deux régions du cerveau : le noyau accumbens et le cortex préfrontal médian, où la méphédrone plus l’éthanol ont potentialisé la libération de DA et de 5-HT par rapport à la méphédrone seule. Dans des études expérimentales, la méphédrone n’a pas compensé les effets des troubles de la mémoire spatiale induits par l’éthanol. En outre, le MDPV avec l’éthanol a eu des effets différents sur la préférence d’activité locomotrice chez les animaux par rapport à la méphédrone seule. La méphédrone et l’éthanol ont significativement augmenté ce paramètre, mais le MDPV a eu un effet opposé. Cela est probablement dû à la diminution des concentrations de MDPV dans le sang et le cerveau au cours des 20 premières minutes suivant l’injection de MDPV et d’éthanol. La nicotine et la méphédrone administrées seules étaient fortement pro-oxydantes, mais ensemble, elles ont diminué l’état oxydatif.
Les études sur la consommation combinée de cathinones de synthèse et de cannabis ou de cannabinoïdes de synthèse sont rares. Des études démographiques ont montré que les cathinones de synthèse sont en fait souvent consommées avec des dérivés de la marijuana. Klavž et al. ont décrit l’intoxication avec survie d’une personne ayant pris au total deux cannabinoïdes synthétiques AB-CHMINACA et AB-FUBINACA et trois cathinones synthétiques alpha-PHP, alpha-PVP et 4-CMC. Malheureusement, les concentrations de ces xénobiotiques n’ont pas été déterminées. D’autres études confirmant analytiquement la consommation combinée de cathinones synthétiques et de cannabis ou de cannabinoïdes synthétiques concernaient des intoxications mortelles. Kraemer et al. ont recueilli des données sur des intoxications mortelles dues à des combinaisons de cathinones synthétiques et de cannabis ou de cannabinoïdes synthétiques. Par exemple, des cas ont été signalés où l’examen a révélé la présence de méthylone et de THC ou de THC-COOH, d’alpha-pyrrolidinooctanophénone (PV-9) et de THC-COOH, ou d’alpha PVP et de THC, ainsi que de 11-OH-THC et de THC-COOH. Au cours de ces intoxications, les symptômes initialement observés comprenaient l’insomnie, la mydriase, la tachycardie et l’absence de réponse aux stimuli douloureux.
Marinetti et Antonides ont détecté du MDPV, de l’α-PVP, de la méthylone, de la pentylone et de la pyrovalérone dans 23 cas. À l’exception d’un cas, où seul le MDPV a été déterminé, il y avait également d’autres cathinones synthétiques, des drogues classiques ou des médicaments. Dans 12 cas, la cause du décès a été déterminée comme une intoxication mixte avec des xénobiotiques détectés. Le MDPV a été détecté dans neuf cas, et dans deux de ces cas, l’intoxication au MDPV était la cause principale du décès. L’alpha-PVP elle-même associée à d’autres substances était présente dans deux cas et dans un cas, la pentylone et l’alpha-PVP ont été trouvées en combinaison avec d’autres xénobiotiques. Malheureusement, les concentrations d’alpha-PVP et de pentylone n’ont pas été déterminées. Dans deux cas d’intoxication au MDPV, les concentrations identifiées de cette substance étaient de 91 ng/ml dans le sang fémoral, 132 ng/ml dans le liquide oculaire, >200 ng/ml dans l’urine (dans le premier cas) et 4 800 ng/g dans le foie (dans le second cas). Il est difficile d’interpréter sans ambiguïté les concentrations de MDPV ci-dessus en raison de la présence d’autres xénobiotiques, c’est pourquoi les cas d’intoxications simples sont les plus précieux. Sur les 11 cas restants, pour lesquels une autre cause de décès a été identifiée, le MDPV était la seule substance identifiée dans un cas. Les concentrations de MDPV étaient de 640 ng/ml dans le sang fémoral, 896 ng/g dans le cerveau, 6080 ng/g dans le foie, 1880 ng/g dans la bile et 940 ng/g dans le liquide oculaire. La cause du décès dans ce cas était une pendaison suicidaire. Ces résultats indiquent que la distribution du MDPV dans l’organisme était toxique mais non létale.
Des conclusions similaires peuvent être tirées d’études de cas où les décès ont été causés par des accidents. Dans un cas, la concentration de MDPV dans le sang du cœur était de 56 ng/ml, alors qu’elle était de 729 ng/ml pour la méthylone. Dans un autre cas, la concentration de pyrovalérone était de 42 ng/ml dans le sang fémoral, 59 ng/ml dans le sang cardiaque, 48 ng/g dans le cerveau, 124 ng/g dans le foie, 1 880 ng/ml dans la bile et 24 ng/ml dans le liquide oculaire. En outre, dans le dernier des cas susmentionnés, de la pentylone a été trouvée dans le sang, mais seule une analyse qualitative a été effectuée.
Ces résultats montrent que la distribution des xénobiotiques dans l’organisme peut être toxique mais pas létale. La connaissance de la distribution des cathinones synthétiques dans les différents tissus de l’organisme peut faciliter la compréhension des mécanismes de leur toxicité. Cependant, ces données sont encore rares dans la littérature professionnelle.
7. Résumé.
Malgré le renforcement et l’évolution des réglementations légales concernant la production, le traitement, la vente et la possession de substances appartenant au groupe des cathinones synthétiques, l’abus de ces composés à des fins récréatives reste élevé. Bien que les premières cathinones synthétiques aient été synthétisées dans les années 1920, une augmentation rapide de la popularité de ces substances sur le marché des drogues illicites a été enregistrée après l’an 2000 et est probablement alimentée par la légalité de ces substances. Les cathinones synthétiques sont toujours très populaires malgré l’absence de recherches scientifiques détaillées sur les effets nocifs de ces substances sur le corps humain. Les problèmes fondamentaux liés aux NPS concernent principalement leur disponibilité et leur administration à grande échelle avec d’autres xénobiotiques, le grand nombre de ces substances et les changements qualitatifs et quantitatifs dynamiques sur le marché de la drogue.
La structure chimique et les cas d’intoxication aux cathinones synthétiques confirmés analytiquement indiquent la similitude d’action (effets cliniques) entre ces composés et l’amphétamine ou la MDMA. Les cathinones synthétiques exercent des effets toxiques non seulement sur le CNS, mais aussi sur le système cardiovasculaire, le tractus gastro-intestinal ou les reins. L’absorption chronique de fortes doses de cathinones synthétiques entraîne le développement d’une tolérance, d’une dépendance et, en cas d’arrêt, de symptômes de sevrage. Dans les cas extrêmes, ces substances peuvent également provoquer une défaillance de plusieurs organes et entraîner la mort. De nombreux décès ont été signalés en relation avec l’utilisation de cathinones synthétiques. L’utilisation de cathinones synthétiques doit être considérée comme une menace sérieuse pour la santé et la vie, et les intoxications par les composés les plus couramment utilisés doivent être surveillées par les unités de toxicologie clinique et les services médico-légaux. Il existe peu de données sur la pharmacodynamique et la pharmacocinétique des cathinones synthétiques chez l’homme, et la compréhension actuelle du problème repose principalement sur un petit nombre d’études in vitro et animales. Des recherches supplémentaires sont nécessaires sur les mécanismes d’action, la toxicocinétique, la toxicodynamie, le métabolisme, les effets cliniques et le potentiel de dépendance des cathinones de synthèse, en particulier dans le contexte des risques potentiels causés par une consommation accrue de ce groupe de médicaments à l’avenir.